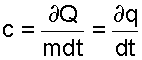
(4.17)
Понятие теплоемкости рассмотрено в разделе 3.2. “Теплота”. Применим это понятие для газов, систематизируя разновидности теплоемкостей.
Удельная массовая теплоемкость - это количество теплоты, необходимое для нагрева 1 кг газа на один градус. Она обозначается буквой с, имеет размерность Дж/(кг·град) и определяется как
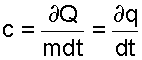 |
(4.17) |
Удельная мольная теплоемкость - это количество теплоты, необходимое для нагрева одного моля (киломоля) газа на один градус. Ее обозначение сμ, размерность Дж/(кмоль·град), расчетное выражение соответствует произведению молярной массы газа на его удельную массовую теплоемкость, т.к. в одном киломоле μ килограммов газа
(4.18) |
Удельная объемная теплоемкость газа - это количество теплоты необходимое для нагрева одного кубического метра газа на один градус. Ее обозначение с', размерность Дж/(м3·град), расчетное выражение соответствует следующим соотношениям
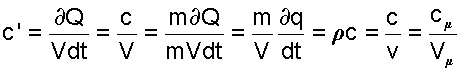 |
(4.19) |
Плотность газа и объем киломоля газа зависят от температуры и давления, поэтому при различных параметрах объемная теплоемкость оного и того же газа различна даже в случае постоянной ее удельной массовой теплоемкости. Для практического пользования такой теплоемкостью необходимо к каждому ее значению указывать соответствующие ему значения температуры и давления газа, что очень неудобно. В справочной литературе принято давать объемную теплоемкость газа, отнесенную к одному кубическому метру газа, взятому при нормальных физических условиях – 0 0С и 760 мм рт.ст. (нм3). При нормальных условиях один киломоль любого идеального газа занимает объем 22,4 м3. При этих условиях удельную объемную теплоемкость идеального газа удобно определять как
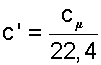 |
(4.20) |
Поскольку теплота является функцией процесса, то и теплоемкость есть функция процесса. На практике наибольшее применение нашли теплоемкости изобарного - cp при Р=const и изохорного - cv при v=const процессов.
| предыдущий параграф | содержание | следующий параграф |