(3.27)
В технической термодинамике в основном рассматривают процессы изменения состояния термодинамического тела, находящегося только в тепловом и механическом взаимодействии с телами внешней среды.
Ранее мы оговорили условие, что все процессы будем рассматривать применительно к закрытым термодинамическим системам (без обмена веществом с окружающей средой). Если термодинамическое тело (система) находится в покое или скорость его движения не меняется, т.е. не меняется его кинетическая энергия видимого движения, а также не меняется положение его центра тяжести по отношению к центру Земли, т.е. не меняется его потенциальная энергия в гравитационном поле Земли, то нет изменения запаса его механической энергии. Результатом его взаимодействия с внешней средой в этом случае является изменение его внутренней энергии. Внутренняя энергия может быть изменена за счет подвода (отвода) к телу теплоты (совершения тепловой работы) и за счет совершения над ним со стороны окружающей среды (или самим телом над окружающей средой) работы изменения объема (механической работы). И то и другое является мерой энергетического взаимодействия тела и внешней среды, мерой передачи телу энергии от внешних источников. Согласно закону сохранения энергии в этой системе изменение ее внутренней энергии будет равно сумме внешних тепловых и механических работ.
Таким образом, аналитическое выражение первого закона термодинамики для замкнутой системы будет иметь вид:
(3.27) |
Штрих указывает на то, что это работа изменения объема действительного необратимого процесса. Подробное изложение о различие работ расширения в обратимых и в необратимых процессах будет приведено в следующем разделе.
В выражении (3.27) знак минус перед работой изменения объема обусловлен правилом знаков, согласно которому принято, что увеличение внутренней энергии тела ( U2-U1>0 ) возможно за счет подводa к нему теплоты (Q имеет знак плюс, согласно его расчетного выражения dQ=TdS при подводе к телу теплоты dS>0 и Q>0) и за счет совершения над ним работы изменения объема со стороны внешней среды (L'- работа изменения объема самого тела, -L' - работа изменения объема внешней среды над телом, согласно расчетного выражения для работы изменения объема обратимого процесса dL=PdV при совершении механической работы над телом со стороны окружающей среды dV<0 и L<0, т.е. в этом случае -L>0).
Очевидно, что изменение внутренней энергии может бать вызвано энергетическим взаимодействием тела с окружающей средой и одного вида: или только механического, или только теплового. Из выражения (3.27) следует принцип эквивалентности работы расширения (механической работы) и теплоты (тепловой работы), т.е. одинаковость их природы, а соответственно и размерности. Вот некоторые из часто встречающихся соотношений:
1 ккал = 4,187 кДж, 1 кВт ч = 3600 кДж = 860 ккал.Длительное время природу теплоты объясняли с помощью ложной теории теплорода. Размерность теплоты была только в калориях, эквивалента теплоты и механической работы не было. Одинаковую природу теплоты и механической работы доказал английский физик Д.Джоуль в 1843-1850 г.г. . Он же определил эквивалент механической и тепловой работы 1 ккал = 427 кГм.
Джоуль провел следующий опыт (рис. 3.6). В замкнутый жесткий сосуд В с газом, исключающий механическое взаимодействие газа и внешней среды путем изменения объема газа, поместили мешалку. Механическое взаимодействие газа с внешней средой (без изменения объема газа) может осуществляться вращением мешалки, приводимой в действие за счет опускания груза А. Тепловое взаимодействие газа с внешней средой может осуществляться с помощью его контакта с телом D, имеющим температуру большую, чем у газа tD>tB.
Изменение состояния газа в сосуде (например, ориентируясь на температуру и давление) можно осуществить двумя способами: механическим - путем вращения мешалки, и тепловым - нагревая газ с помощью тела D (рис.3.6а). В обоих случаях будет происходить изменение внутренней энергии газа. Джоуль добился одинакового изменения состояния газа механическим и тепловым взаимодействием газа с внешней средой, т.е. в начале и в конце каждого энергетического взаимодействия параметры газа были одинаковы, например P1 и t1, P2 и t2. Поскольку одинаковы начальные и конечные состояния газа в обоих опытах, то одинаково и изменение внутренней энергии газа в этих опытах. Исходя из этого, можно записать
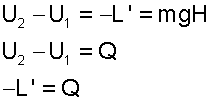 |
(3.28) |
В соответствии с выражением (3.28) получили эквивалентность механической работы, произведенной над газом и теплоты, подведенной к газу.
Размерности теплоты и механической работы расширения в системе СИ одинаковы - Дж, поэтому в данной системе единиц выражение первого закона термодинамики не требует ввода эквивалента между единицами теплоты и работы, как это делалось во времена Джоуля.
| предыдущий параграф | содержание | следующий параграф |