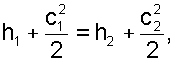
(5.1)
Дросселированием называется необратимый процесс снижения давления, без совершения технической работы и без изменения кинетической энергии видимого движения потока вещества.
Процессы дросселирования имеют место при регулировании и измерении расходов рабочих тел, снижении их температур и давления и т.д. Процесс дросселирования обусловлен наличием препятствия на пути движения потока по каналу, которое вызывает деформацию (мятие) потока.
Рассмотрим наиболее наглядный пример дросселирования потока газа (пара) в канале трубопровода, разделённом перегородкой с отверстием малого размера по отношению к поперечному сечению канала, такие перегородки носят название диафрагмы (рис. 5.1).
Диафрагмы используются для измерения расхода вещества, движущегося по каналу.
Площади поперечного сечения канала до и после перегородки одинаковые. При прохождении потока через малое отверстие диафрагмы поток сужается, скорость его растёт, давление и энтальпия понижаются, аналогично истечению через сопло. За узким сечением поток расширяется и на достаточно удалённом расстоянии от диафрагмы заполняет всё сечение и происходит торможение потока, при этом уменьшается скорость, растёт энтальпия и повышается давление. В мертвых зонах до и после диафрагмы, образуются вихревые потоки, вызывающие потери давления и работоспособности рабочего тела.
Поскольку процесс дросселирования быстротечен, его можно считать, идущим без теплообмена с окружающей средой q=0. В этом процессе практически отсутствует изменение кинетической энергии потока, т.к. площади сечений канала одинаковы, а увеличение удельного объема газа за счет снижения давления уменьшает кинетическую энергию потока на очень малую величину по отношению к численным значениям энтальпий, поэтому считают, что c1=c2. Нет совершения технической работы lТ=0 и нет работы изменения давления в потоке lО=0. Уравнение первого закона термодинамики для 1 и 2 сечений канала (до и после дросселирования) будет иметь вид:
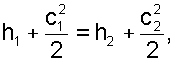 |
(5.1) |
(5.2) |
Таким образом, в результате адиабатного процесса дросселирования энтальпия вещества в начале и конце процесса одинакова. При этом необходимо отметить, что это не изоэнтальпный процесс. Энтальпия вещества при дросселировании в промежуточных состояниях этого процесса изменяется, но конечное значение энтальпии при дросселировании не зависит даже от того, за счёт чего происходит дросселирование, вызвано ли оно клапаном, диафрагмой, пористой перегородкой и т.п. Конечное состояние вещества при адиабатном дросселировании и при c1=c2 определяется значениями начальной энтальпии и величиной конечного давления.
Наглядно продемонстрировать физическую природу снижения давления в процессе дросселирования можно условно разбив процесс дросселирования на два необратимых адиабатных процесса (рис.5.2): 1-ый – расширения (как в сопле) и 2-ой – сжатия (как в диффузоре). Необратимость адиабатных процессов 1А и А2 смещает точку 2 в область Р2<Р1 при h1=const.
Таким образом, адиабатный процесс дросселирования есть необратимый процесс (DSС>0) снижения давления вещества без совершения им работы изменения давления потока и без изменения энтальпии. При этом нельзя путать понятие адиабатного процесса дросселирования с изоэнтропным (s=const) – адиабатным процессом. Дросселирование это типичный необратимый процесс с увеличением энтропии системы и потерей работоспособности – эксергии рабочего тела.
| предыдущий параграф | содержание | следующий параграф |