(9.23)
Рассмотрим процесс обратимого теплообмена между двумя телами, имеющими одинаковую постоянную температуру Т1 (рис. 9.16). В обратимом теплообмене отсутствует разница температур между процессом передачи теплоты одним телом и процессом получения теплоты вторым телом. Первое тело (1т) отдает теплоту Q (процесс 12) и его энтропия уменьшается на величину ΔS1 = Q/T1. Второе тело (2т), согласно первому закону термодинамики, получает то же количество теплоты (процесс 21), но с обратным знаком -Q, и его энтропия увеличивается на величину ΔS2 = - ΔS1 = -Q/T1, так как обратимый процесс получения теплоты идет по траектории 21, совпадающей с процессом отвода теплоты 12. Суммарное изменение энтропии этой системы равно нулю.
(9.23) |
Выражение (9.23) справедливо для любого случая обратимого теплообмена. Так, при переменной температуре двух тел в случае обратимого теплообмена между ними (рис.9.17), получаем изменение энтропии этой системы тоже равное нулю
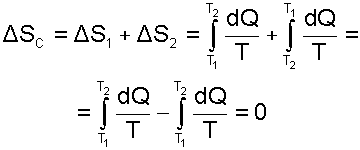 |
(9.24) |
Таким образом, при обратимом теплообмене энтропия системы не изменяется.
Реальный процесс теплообмена между телами происходит при конечной разности температур и поэтому необратим.
Рассмотрим теплообмен между двумя телами, имеющими постоянные температуры Т1 и Т2 (рис.9.18). Первое тело отдает теплоту Q (процесс 12), а второе (процесс 34) получает теплоту - Q. Изменение энтропии системы в этом случае будет больше нуля, так как Т1>T2, а Q>0.
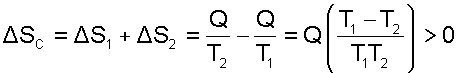 |
(9.25) |
Аналогичная ситуация будет и при необратимом теплообмене между телами с переменной температурой (рис. 9.19), такой процесс возможен в поверхностном теплообменнике. Таким образом, при необратимом теплообмене энтропия системы возрастает.
| предыдущий параграф | содержание | следующий параграф |