Сначала договоримся, что под термином "вода" будем понимать Н2О в любом из возможных ее фазовых состояний.
В природе вода может быть в трех состояниях: твердой фазе (лед, снег), жидкой фазе (вода), газообразной фазе (пар).
Рассмотрим воду без энергетического взаимодействия с окружающей средой, т.е. в равновесном состоянии.
У поверхности льда или жидкости всегда находится пар. Соприкасающиеся фазы находятся в термодинамическом равновесии: быстрые молекулы вылетают из жидкой фазы, преодолевая поверхностные силы, а из паровой фазы медленные молекулы переходят в жидкую фазу.
В состоянии равновесия каждой температуре соответствует определенное давление пара - полное (если над жидкостью только пар) или парциальное (если присутствует смесь пара с воздухом или другими газами). Пар, находящийся в равновесном состоянии с жидкой фазой, из которой он образовался, называется насыщенным паром, а соответствующая ему температура называется температурой насыщения, а давление - давлением насыщения.
Неравновесное состояние воды:
а) Механически неравновесное состояние. Пусть понижается давление пара над жидкостью ниже давления насыщения. В этом случае нарушается равновесие, происходит некомпенсированный переход вещества из жидкой фазы в газообразную через поверхность раздела фаз за счет наиболее быстрых молекул.
Процесс некомпенсированного перехода вещества из жидкой фазы в газообразную называется испарением.
Процесс некомпенсированного перехода вещества из твердой фазы в газовую называется сублимацией или возгонкой.
Интенсивность испарения или сублимации возрастает при интенсивном отводе образующегося пара. При этом понижается температура жидкой фазы за счет вылета из нее молекул с наибольшей энергией. Этого можно добиться и без понижения давления, просто обдувом поверхности жидкости потоком воздуха.
б) Тепловая неравновесность. Пусть идет подвод теплоты к жидкости, находящейся в открытом сосуде. При этом температура, а соответственно и давление насыщенного пара над жидкостью растет и может достигнуть полного внешнего давления (Р=РН). В случае, когда Р=РН, у поверхности нагрева температура жидкости поднимается выше температуры насыщенного пара при господствующем здесь давлении, т.е. создаются условия образования пара в толще жидкости.
Процесс перехода вещества из жидкой фазы в паровую непосредственно внутри жидкости называется кипением.
Процесс зарождения пузырьков пара в толще жидкости сложен. Для кипения воды необходимо наличие центров парообразования на поверхности подвода теплоты - углубления, выступы, неровности и т.п. У поверхности нагрева, при кипении, разность температур воды и насыщенного пара при господствующем здесь давлении зависит от интенсивности подвода теплоты и может достигать десятков градусов.
Действие сил поверхностного натяжения жидкости обусловливает перегрев жидкости на поверхности раздела фаз при ее кипении на 0,3-1,5 градуса по отношению к температуре насыщенного пара над ней.
Любой процесс перехода вещества из жидкой фазы в паровую называется парообразованием.
Процесс, противоположный парообразованию, т.е. некомпенсированный переход вещества из паровой фазы в жидкую, называется конденсацией.
При постоянном давлении пара конденсация происходит (как и кипение) при постоянной температуре и является результатом отвода теплоты от системы.
Процесс, противоположный сублимации, т.е. переход вещества из паровой фазы непосредственно в твердую, называется десублимацией.
Напомним, что введенные ранее понятия насыщенного пара и температуры насыщения, перенесенные на процесс кипения, приводят к равенству температур пара и жидкости. В этом случае и давление и температура жидкой и паровых фаз одинаковы.
Жидкая фаза воды при температуре кипения называется насыщенной жидкостью.
Пар при температуре кипения (насыщения) называется сухим насыщенным паром.
Двухфазная смесь "жидкость+пар" в состоянии насыщения называется влажным насыщенным паром.
В термодинамике этот термин распространяется на двухфазные системы, в которых насыщенный пар может находиться над уровнем жидкости или представлять смесь пара с взвешенными в нем капельками жидкости. Для характеристики влажного насыщенного пара используется понятие степени сухости х,представляющее собой отношение массы сухого насыщенного пара, mС.Н.П., к общей массе смеси, mСМ = mС.Н.П. + mЖ.С.Н. , его с жидкостью в состоянии насыщения:
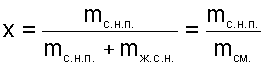 |
(7.1) |
Отношение массы жидкости воды в состоянии насыщения к массе смеси называется степенью влажности (1-х):
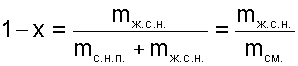 |
(7.2) |
Подвод теплоты к влажному насыщенному пару при постоянном давлении приводит к переходу жидкой фазы смеси в паровую. При этом температура смеси (насыщения) не может быть повышена до тех пор, пока вся жидкость не будет превращена в пар. Дальнейший подвод теплоты только к паровой фазе в состоянии насыщения приводит к повышению его температуры.
Пар с температурой выше температуры насыщения при данном давлении называется перегретым паром. Разность температур перегретого пара t и насыщенного пара того же давления tН называется степенью перегрева пара DtП = t -tН.
С увеличением степени перегрева пара его объем растет, концентрация молекул уменьшается, по своим свойствам он приближается к газам.